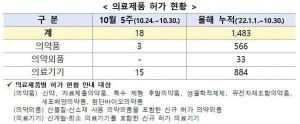
행정·법령·정책 목록 ( 총 : 2,717건)
-
-
식약처, '영유아용 코로나19 화이자사 백신' 허가…한국화이자제약 신청 '영유아(6개월~4세)용 코로나19 초기 바이러스 백신' 수입품목 '코미나티주0.1mg/mL(6개월-4세용)(토지나메란)' 허가
-
식약처, '백신·혈장분획제제 품질관리 최신 정보' 공유…식약처, '생물학적제제 품질관리실험실 네트워크(Lab-Net) 워크숍' 개최
-
-
-

-

-
식약처, '페나리딘(Phenaridine)' 임시마약류 지정 예고…'오·남용 우려되는 신종·불법 물질 관리' 강화
-
-

-
-
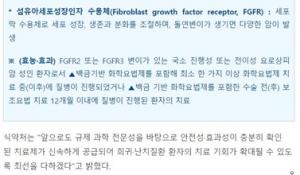
식약처, '만성 신장질환 환자 빈혈 치료제 선택권' 확대…제이더블유중외제약 '에나로이정(에나로두스타트)' 3개 용량 허가
-
-

-
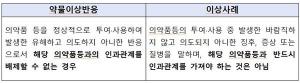
식약처, '의사 본인 과다 처방' 등 '마약류 부적정 취급' 집중 점검…식약처·경찰청·심평원, '의료용 마약류 기획합동점검' 실시
-
'2022년 하반기 국제의약품규제조화위원회' 인천서 개최…'ICH 정기총회 처음으로 국내 개최' 20개 회원국·36개 참관국 대표 참석
-
-

-

-

-
-
식약처, '국제 규제기관 실무자 바이오의약품 GMP 교육' 실시…'2022년 WHO GLO GMP 조사관 대상 역량강화 교육' 운영
-

-

-

-