한국MSD '키트루다'의 임상연구'KEYNOTE-024' 결과, 항암화학요법 대비 질병 진행의 위험 혹은 사망률을 50% 감소시켰고, 사망 위험은 40% 감소한 것으로 나타났다. '키트루다'는 비소세포폐암 1∙2차 치료에서 모두 사용가능한 면역항암제로 제시됐다.
'국내 위험 분담제 현황'의 경우, 위험 분담 계약 약제 중 급여 확대가 이루어진 사례로 얼비툭스(머크), 레블리미드(세엘진), 잴코리(한국화이자제약), 키트루다(한국MSD), 옵디보(한국오노약품공업·한국BMS제약) 등이 제시됐다.
한국MSD는 26일 서울스퀘어에서 '비소세포폐암 1차 표준치료제로서 면역항암제의 의의와 치료환경 전망'을 주제로 'Media Education Session'이 진행됐다.
이날 세션에서 ▲한국MSD 의학부 김영민 이사의 '면역항암제 키트루다의 비소세포폐암 1차 치료제로서 효과와 의의', ▲한국MSD 대외협력부 명혜진 과장의 '국내 위험 분담제 현황' 등에 대해 발표됐다.

키트루다는 최근 흑색종, 비소세포폐암과 더불어 두경부암, 호지킨림프종, 요로상피암 등의 치료제로 허가를 받으며, 총 5개 암종에서 8개 단독 및 병용요법 치료제로 사용이 가능해졌다.
이날 한국MSD 의학부 김영민 이사<메디컬헤럴드 사진>는 "키트루다는 비소세포폐암 1∙2차 치료에서 모두 사용가능한 면역항암제"라고 말했다.
김영민 이사는 '키트루다 임상연구(KEYNOTE-024) 결과' 강연을 통해 "키트루다가 항암화학요법 대비 질병 진행의 위험 혹은 사망률을 50% 감소시켰고, 사망 위험은 40% 감소했다"고 말했다.

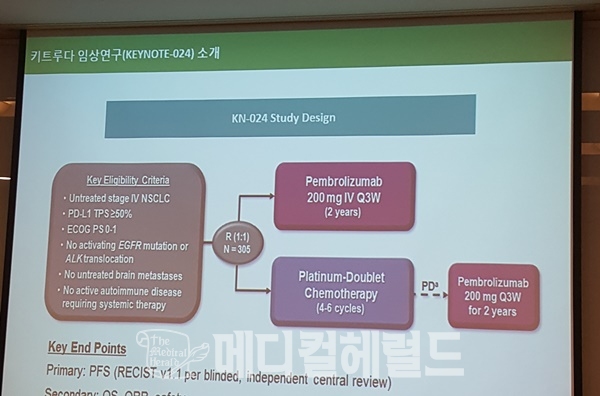
메디컬헤럴드가 'KEYNOTE-024 임상 시험' 자료를 확인한 결과, 'KEYNOTE-024' 임상시험은 기존 치료 경험이 없고 PD-L1 발현율이 높은(TPS≥50%) 305명의 환자를 대상으로 표준 요법인 백금 기반의 2제 요법(페메트렉시드+카보플라틴, 페메트렉시드+시스플라틴, 젬시타빈+시스플라틴, 젬시타빈+카보플라틴, 파클리탁셀+카보플라틴)과 키트루다(200 mg, 3주 1회)의 효과를 비교하기 위한 무작위, 오픈 라벨 3상 연구인 것으로 나타났다.
| 'KEYNOTE-024' 임상 시험 기존 치료 경험이 없고 EGFR 또는 ALK 변이가 없으며, 동반진단 'PD-L1 1HC 22C3 PharmDx test'를 통해 PD-L1 발현율이 50% 이상인 환자를 대상으로 진행됐다. 해당 연구에서 환자 스크리닝 시 30.2%(n=500/1653)의 종양 샘플은 PD-L1 발현율이 50% 이상으로 확인됐다. 1차 유효성 평가 기준은 무진행 생존기간(PFS), 2차 평가 기준은 전체 생존기간(OS), 전체 반응률(ORR), 및 안전성(Safety)이었다. 연구 결과, 키트루다가 항암화학요법 대비 질병 진행의 위험 혹은 사망률을 50% 감소시켰고(HR, 0.50 [95% CI, 0.37, 0.68]; p<0.001), 사망 위험은 40% 줄였다.(HR, 0.60 [95% CI, 0.41, 0.89]; p=0.005) 반응률의 경우, 키트루다 투여군이 44.8%(95% CI, 36.8 to 53.0)로, 27.8%(95% CI, 20.8 to 35.7)인 항암화학요법 투여군에 비해 높은 것으로 확인됐고, 치료제 관련 부작용 역시 더 적게 나타났다.(73.4% vs 90.0%) |
한국MSD 대외협력부 명혜진 과장<사진>은 위험분담제도 도입 배경에 대해 "선별급여등재 제도 하에서 비용효과성을 입증할 수 없거나 협상이 결렬되어 비급여 되는 고가의 항암

제, 희귀난치질환 치료제의 환자 접근성 문제 대두와 정부의 4대 중증질환 보장성 강화 정책의 일환으로 항암제와 희귀난치질환 치료제의 보험급여를 높여야 할 필요성이 작용됐다"고 말했다.
한국MSD 대외협력부 명혜진 과장은 '위험분담계약 기간 내 급여 기준 확대'를 설명하며, 위험분담계약 약제 중 급여 확대가 이루어진 사례는 '얼비툭스'(머크), '레블리미드'(세엘진), '잴코리'(한국화이자제약), '키트루다'(한국MSD), '옵디보'(한국오노약품공업·한국BMS제약) 등이 해당된다고 밝혔다.

