식품의약품안전처(이의경 처장)은 국내 개발 코로나19 항체치료제 ‘CT-P59’에 대해 1상 임상시험을 17일 승인했다고 밝혔다.
이번에 승인한 'CT-P59'는 ‘셀트리온’에서 신약으로 개발 중인 유전자재조합 항체치료제로, 건강한 사람을 대상으로 안전성 등을 평가하는 1상 임상시험을 진행하게 된다.

이번 1상 시험에서는 안전성을 확인하고, 이후 환자 대상으로 2상 및 3상 시험을 거쳐 안전성과 유효성이 확보돼야 품목허가가 가능하다.
치료 원리는 코로나19 바이러스가 인체 세포와 결합하는 부위에 항체치료제가 대신 붙음으로써 감염을 막게 된다.
이로써 현재 국내에서 코로나19 관련해 진행 중인 치료제 및 백신의 임상시험은 총 13건(치료제 11건, 백신 2건)이다.
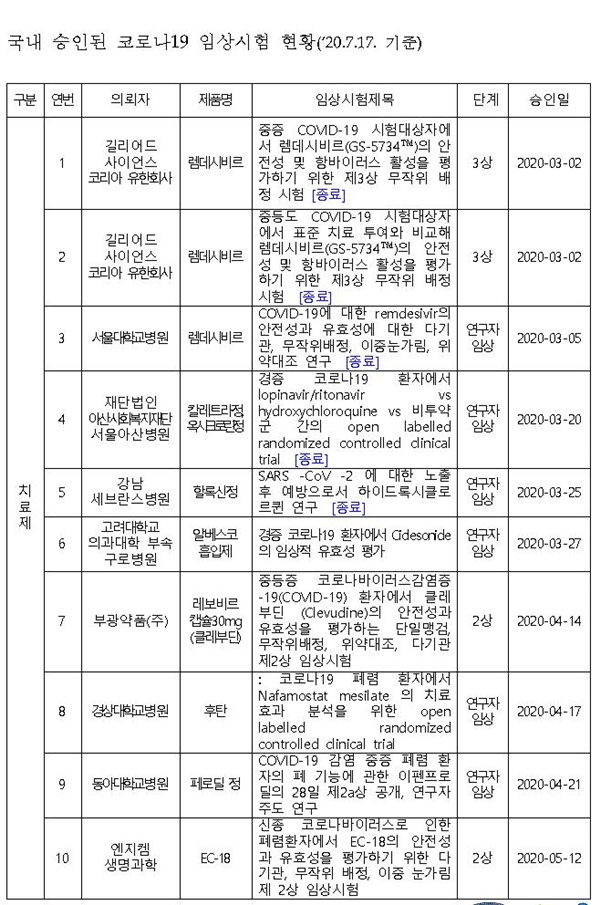
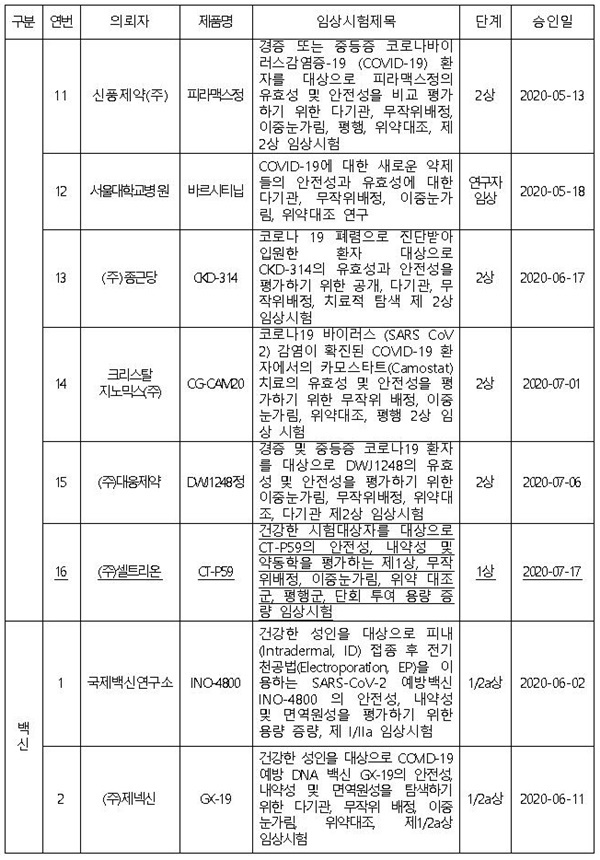
식약처에 따르면, 국내 승인된 코로나19 치료제 임상시험<下 표 참조>의 경우, 고려대구로병원 알베스코흡입제 연구자 임상, 부광약품 '레보비르캡슐30mg'(클레부딘) 2상, 신풍제약 '피라맥스정' 2상, 서울대병원 바르시티닙 연구자임상, 종근당 'CKD-314' 2상, 대웅제약 'DWJ1248정' 2상 등이 해당된다.
국내 승인된 코로나19 백신 임상시험<표 참조>의 경우, 국제백신연구소 INO-4800 1/2a상 , 제넥신 GX-19 1/2a상 등 2건이 해당된다.
식약처는 "코로나19 치료제·백신 개발에 대한 국민적 관심이 높은 만큼 앞으로도 개발 제품의 임상시험 현황에 대해서 신속하게 정보를 전달하겠다"며 "안전하고 효과 있는 코로나19 치료제·백신이 신속히 개발될 수 있도록 필요한 사항을 지원하고 우리 국민의 치료 기회를 보장할 수 있도록 최선을 다할 계획"이라고 밝혔다.

