| 한국얀센社의 '코비드-19백신 얀센주'의 예방 효과에 대해 검증 자문단은 제출된 자료에서 18세 이상 1회 투여 14일 후와 28일 후 효과가 확인됐으며, 면역반응(결합항체 및 중화항체)이 12주까지 유지되고 있어 허가를 위한 예방 효과는 인정 가능하다고 판단했다. 임상시험에서 발생한 이상사례와 관련해 검증 자문단은 임상시험에서 안전성 프로파일(경향성)은 허용할 만한 수준으로 판단했다. |
식품의약품안전처(처장 김강립)는 한국얀센社의 '코비드-19백신 얀센주' 품목허가 진행 상황에 대해 29일 발표했다.
식약처는 한국얀센의 '코비드-19백신 얀센주'의 임상시험 결과에 대해 '코로나19 백신 안전성·효과성 검증 자문단'(이하 검증 자문단) 회의를 3월 28일 개최했다.
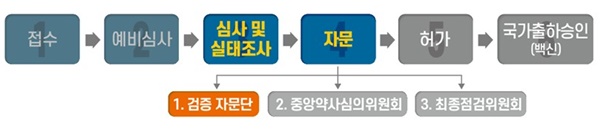
검증 자문단은 중앙약사심의위원회 자문에 앞서 식약처가 임상·비임상·품질 등 다양한 분야의 전문가들에게 자문 의견을 수렴하는 절차로서 이번 검증 자문단 회의에는 감염내과 전문의, 백신 전문가 및 임상 통계 전문가 등 6명이 참석했다.
◆임상시험 결과= 제출된 임상 시험 자료는 미국과 벨기에(1·2상)에서 수행된 임상시험 1건, 일본(1상) 1건, 독일 등 다국가(2상) 1건, 미국 등 8개국(3상)에서 수행된 다국가 임상시험 1건 등 총 4건으로, 안전성과 효과성은 미국 등에서 수행된 3상 임상시험을 통해 평가했다.
미국 등에서 수행된 임상시험에서 백신 또는 대조약물을 투여받은 사람은 4만 3,783명으로 평균연령은 50.7세이며, ▲여성 45%(1만 9,722명) ▲비만·고혈압·당뇨 등 기저질환이 있는 사람 40.8%(1만 7,858명) ▲65세 이상 19.6%(8,561명)가 포함됐다.
예방 효과의 경우, 백신 또는 대조약(생리식염수 0.9%)을 코로나19 감염이 확진되지 않은 3만 9,321명(백신군 1만 9,630명, 대조군 1만 6,915명)을 대상으로 투여해 평가했다.
예방 효과는 백신 또는 대조약물을 1회 투여한 후 각각 14일과 28일 이후 각 군에서 발생한 코로나19 감염 환자의 비율을 비교·분석한 것으로 코로나19 임상증상이 있고, 코로나19 바이러스 검사 결과 양성이 확인된 경우 감염이 확진된 것으로 정의했다.
| * RT-PCR(역전사 중합효소 연쇄반응 분자진단법, Reverse Transcription Polymerase Chain Reaction) : Abbott Real Time SARS-CoV-2 RT- PCR assay |
평가 결과, 코로나19로 확진 받은 사람은 백신 투여 14일 이후 백신군 116명, 대조군 348명으로 약 66.9%의 예방 효과가 나타났고, 28일 이후에는 백신군 66명, 대조군 193명으로 약 66.1%의 예방 효과를 보였으며, 백신 투여 14일 후 연령, 기저질환 유무에 관계없이 60% 이상의 예방 효과가 있었다.
또한, 중증의 코로나19 예방에 대해서는 백신 투여 14일 이후 백신군 14명, 대조군 60명으로 약 76.7%, 백신 투여 28일 이후 백신군 5명, 대조군 34명으로 약 85.4% 예방 효과가 있었다.
면역원성 평가의 경우, 백신효과를 예측할 수 있는 간접 지표로써 백신 투여 후 몸 안에 생성되는 항체의 종류와 양 등 면역반응을 평가했다.
코로나19 바이러스 항원과 결합하는 '결합항체'의 경우 투여 전과 비교했을 때 백신 투여 4주 후부터 '항체가'가 4배 이상 증가하는 대상자 비율 등을 의미하는 ‘혈청전환율’이 95%이상이었다.
또한, 바이러스 입자표면에 결합해 바이러스의 감염성을 중화시킴으로써 예방 효과를 유도할 수 있는 ‘중화항체’의 경우에도 백신 1회 투여 후 ‘혈청전환율’은 90% 이상이었다.
안전성의 경우, 백신 접종 후 예측되는 이상사례(국소, 전신)는 총 6,736명(백신군: 3,356명, 대조군: 3,380명)을 대상으로 백신 투여 후 7일간 조사했다.
국소 반응은 주사부위통증(48.7%), 홍반(7.3%), 종창(5.3%)으로 대부분 경증에서 중간 정도이며 발생 후 2~3일 이내에 소실됐다. 전신반응은 두통(39.0%), 피로(38.3%), 근육통(33.2%), 오심(14.2%), 발열(9.0%) 순으로 대부분 경증에서 중간 정도이며, 접종 후 1~2일내 발생하여 1~2일 이내에 소실됐다. 대부분 국소·전신반응 모두 성인에 비해 65세 이상 고령자에서 발생빈도와 중증도가 낮았다.
백신 투여와 관련성이 있는 예측되지 않은 이상사례(투여 후 4주간 조사)는 백신군의 약 7.2%(242/3,356명)에서 발생했으며 주요 증상은 오한(1.7%), 코막힘(0.3%), 관절통(0.5%), 기침(0.4%), 설사(0.3%) 등이었다.
고령자에서의 이상사례 발생빈도는 성인에 비해 낮은 수준으로 전반적으로 연령, 인종, 기저질환에 따른 차이는 보이지 않았다.
아울러, 임상시험의 모든 등록대상자 4만 3,783명 중 백신군 0.4%(83명), 대조군 0.4%(96명)에서 ‘중대한 이상사례’가 보고됐으며, 백신 투여와 관련성을 배제할 수 없는 ‘중대한 약물이상반응’은 상완신경근염 등 7건이었으며, 임상시험 자료 제출 시점에는 대부분 회복중이었다.
◆자문 내용·결과= 검증 자문단 회의에서는 '코비드-19백신 얀센주' 임상시험 자료 등을 바탕으로 안전성 및 유효성에 대한 전반적인 견해, 허가 후 안전성 확보방안 등에 대해 심도 있게 논의했다.
백신의 예방 효과에 대해서 검증 자문단은 제출된 자료에서 18세 이상 1회 투여 14일 후와 28일 후 효과가 확인됐으며, 면역반응(결합항체 및 중화항체)이 12주까지 유지되고 있어, 허가를 위한 예방 효과는 인정 가능하다고 판단했다.
임상시험에서 발생한 이상사례와 관련해 검증 자문단은 임상시험에서 안전성 프로파일(경향성)은 허용할 만한 수준으로 판단했다.
또한, 허가 후 '위해성관리계획'을 통해 임상시험 중 나타난 이상 사례 등을 추가로 관찰하고 정보를 수집해 평가하는 것이 타당하다는 의견이었다.
식약처는 "코로나19 치료제·백신의 허가심사 과정에 있어 다양한 전문가 의견을 수렴해 객관성과 투명성을 확보하는 한편, 철저한 허가·심사가 이뤄질 수 있도록 노력하겠다"고 밝혔다.
식약처는 한국얀센의 '코비드-19백신 얀센주'와 관련해 품질자료 등 심사를 진행하고 이번 '검증 자문단' 자문회의를 통해 얻은 전문가 의견 및 권고사항과 심사 결과를 종합해 신청 품목의 안전성, 효과성, 허가 시 고려해야 할 사항 등에 대해 4월 1일에 식약처 법정 자문기구인 '중앙약사심의위원회'에서 자문받고, 그 결과를 당일 오후에 공개할 예정이다.

