식품의약품안전처(처장 오유경)는 의료제품 허가심사에 대한 투명성과 신뢰성을 강화하기 위해 1월 1주(1월 1일~1월 8일.) 기간 의료제품 허가 현황을 제공한다고 11일 밝혔다.
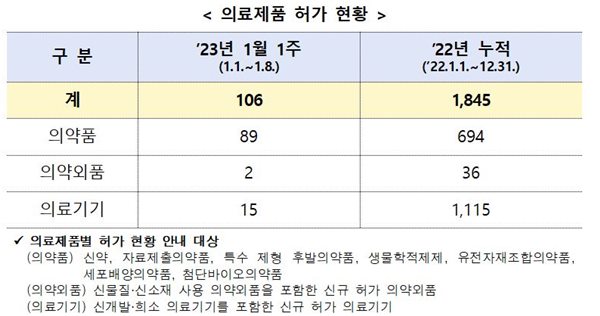
식약처(본부)는 1월 1주(1월 1일~1월 8일.)에 의료제품 총 106개 품목을 허가했다. (2023년 누적: 총 106개 품목)
1월 주에 류마티스관절염, 크론병 등의 치료에 사용되는 동등생물의약품(아달리무맙, 유전자재조합)인 ‘아달로체프리필드시린지주40mg/0.4mL’와‘아달로체펜주40mg/0.4mL’(삼성바이오에피스, ’23.1.3.)를 허가했다.
1월 1주 의료제품 허가 품목 리스트 의약품 현황에 따르면, 자누리틴콤비서방정50/750 밀리그램(대원제약), 테카비어디정(테노포비르알라페나미드)(제일약품), 다포진엠서방정10/1000밀리그램(삼진제약), 듀카노바정30/2.5밀리그램(피마사르탄, 에스암로디핀)(대웅바이오), 올리스탯정60밀리그램(오르리스타트)(대화제약), 포시플듀오서방정10/1000밀리그램(동화약품) 등이 포함됐다.
식약처는 “앞으로도 의료제품 허가 현황을 정례적으로 매주 제공하겠으며, 의료제품별 상세한 허가사항은 전자민원시스템에서 확인할 수 있다”고 밝혔다.
이어 “앞으로도 허가와 관련된 국민 관심이 높은 정보를 적극 발굴해 공개·제공하는데 최선을 다하겠다”고 했다.

