최근 국내 연구진에 의해 암 치료 부작용을 최소화하는 ‘자기(magnetic) 온열 치료법’을 가능하게 하는 새로운 나노입자가 개발됐다.
서울대병원 신경외과 백선하 교수 · 서울대 융합과학기술대학원 박원철 교수·임형준 교수 공동 연구팀은 암 온열치료에 유용한 브로마이드-산화철 나노입자를 개발했다고 17일 밝혔다. 이 입자는 기존에 사용되던 산화철 나노입자보다 우수한 치료 효과를 보이는 것으로 나타났다.
암 치료에 있어 나노입자를 활용한 자기 온열 치료법은 암세포 주변의 정상세포에 영향을 주지 않고 암세포만 국소적으로 치료하는 것을 목표로 한다. 이를 위해서는 적은 양의 입자로도 충분한 열을 발생시킬 수 있어야 한다.
자성 나노입자의 열 전달은 특정 열 흡수율로 결정되는데, 코발트나 망가니즈 등의 중금속은 높은 열 흡수율을 갖는 자성체이지만 인체에 독성을 유발할 수 있다. 이에 연구팀은 중금속을 대신할 수 있는 산화철 나노입자에 주목했다. 산화철 나노입자는 둥글지 않고 각이 있는 형태로, 비등방성(방향에 따라 물질의 물리적 성질이 다른 것)을 증가시켜주면 열효율이 증가한다.
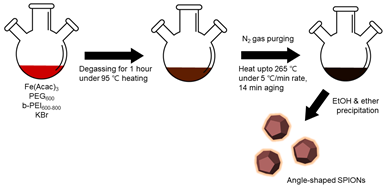
연구팀은 산화철 나노입자의 크기 및 모양에 따른 자기 특성(magnetic properties)을 개선하기 위해 브롬화칼륨(KBr)을 이용해 다양한 각을 갖는 입자를 합성했다. 이때 사용된 용매는 PEI와 PEG로, 다른 유기용매를 사용하는 합성법에 비해 독성이 덜한 특징을 갖는다. 이후 연구팀은 합성된 이 입자들에서 열효율이 증가한다는 사실을 확인했다.
특히 적정량(333.3mM)의 브롬화칼륨을 합성한 입자에서는 약 23℃의 발열효과를 나타냈고, 이는 암세포 치료에 충분한 열이었다.
또한, 연구팀은 나노입자의 독성을 확인하기 위해 세포 실험을 시행했는데, 암세포(U87MG-GFP, Fsall-GFP)에 비해 일반 세포(HFB-141103)에서 독성이 덜한 것으로 나타났다. 이 세 가지 세포 모두 나노입자 100μg/ml 농도까지는 독성이 없었다.
이어 추가로 실시한 교류 자기장 내 암세포 생존 테스트에서 △나노입자(NP) △교류자기장(AMF) △나노입자+교류자기장(NP+AMF) 그룹 중, 나노입자+교류자기장(NP+AMF) 그룹에서 암세포의 성장이 가장 더딘 효과를 보였다.

백선하 교수는 “이번에 개발된 브로마이드-산화철 나노입자는 온열 암 치료에서 좋은 성능을 보일 것으로 예상된다”라며 “전임상 실험에서 좋은 결과를 얻게 되면 임상 적용에 한 걸음 더 나아갈 것”이라고 연구의의를 밝혔다.
박원철 교수는 “브로마이드-산화철 나노입자는 브로마이드 농도에 따라 상이한 광열 변환 효율을 보였고 KBr의 농도가 333.3mM일 때 가장 높은 수치를 보였다”며 “반복된 실험에서도 동일한 성능을 유지한 것을 봤을 때 안정된 나노입자임을 확인했다”고 말했다.
임형준 교수는 “향후 해당 나노입자의 표면에 방사성 동위원소를 포함하는 작용기를 추가 첨가하면 더 좋은 진단 및 치료용 나노입자로 개발할 수 있을 것”이라고 말했다.
한편, 이번 연구 결과는 나노분야 국제 학술지 ‘RSC Advances(IF: 4.036)’ 최신호에 게재됐다.

