|
올해 상반기 승인된 생동성시험의 주요 특징은 ▲심혈관계의약품, 소화계의약품 개발 활발 ▲재심사 또는 특허 만료예정 의약품 개발 집중 등이다.
치료영역별로는 심혈관계 의약품 가장 많아
치료영역별 승인건수는 고령화 및 서구화된 식습관등에 따른 만성질환 증가로 심혈관계의약품 14건(27.5%), 정신신경계의약품 11건(21.6%), 소화계의약품 8건(15.7%)순으로 개발이 활발히 이루어 지고 있는 것으로 나타났다.
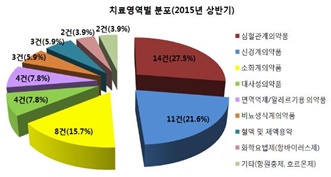
심혈관계 의약품 및 정신신경계의약품 개발은 매년 꾸준히 이루어지고 있으며, 올 상반기 승인건수의 약 절반정도를 차지한다.
소화계의약품의 경우 지난 14년 상반기 5건(6.6%)에서 올해는 8건(15.7%)로 증가했으며, 이는 지난해 특허 만료된 의약품이 집중되면서 제네릭 개발이 활기를 띈 것으로 보인다.
재심사 또는 특허 만료 예정 의약품 개발 집중
올해 상반기 승인된 51건 중 재심사 또는 특허 만료예정인 오리지널품목에 대한 제네릭의약품 생동성승인은 32건(63%)을 차지하는 것으로 분석됐다. 성분별로는 2014년 특허가 만료된 에스오메프라졸마그네슘이 가장 많이 승인(4건, 7.8%)되었으며 파킨슨병 치료제인 레보도파/카르비도파/엔타카폰(3건, 5.9%) 복합제가 그 뒤를 이었다.
'타다라필' 등 특허만료에 힘입어 2014년 상반기 11건(14.5%)에 큰 폭으로 개발 증가했던 비뇨생식기계 의약품의 경우, 올해 상반기에는 3건(5.9%)으로 감소하는 추세를 보였다.
|

