보고건수 증가는 의약품 부작용 피해구제 제도의 점진적 확대 시행(2015년 사망비, 2016년 장례비, 2017년 진료비)과 지역의약품안전센터(27개소)의 부작용 보고 필요성에 대한 홍보, 운영실적이 높은 센터에 운영비를 차등 지급하는 등 부작용 보고 활성화 정책도 영향을 미친 것으로 분석된다.
식약처에 보고된 '의약품 안전성 정보'는 한국의약품안전관리원을 통해 보고 받고 있으며, 해당 의약품과 인과관계 여부와 관계없이 이상사례 의심약물로 보고된 것으로 보고 내용만으로 특정 약물에 의해 부작용이 발생했다고 확정할 수 없는 정보를 말한다.
보고건수는 2012년(92,375건)→2013년(183,260건)→2014년(183,554건)→2015년(198,037건) →2016년(228,939건) 등으로 나타났다.
|
'해열진통소염제'가 31,104건(13.6%)으로 가장 많았고, '항악성종양제' 21,348건(9.3%), '항생제' 18,441(8.1%), 'X선 조영제' 18,240건(8.0%), '합성마약' 17,755건(7.8%) 등의 순이었다.
증상별로는 '오심' 39,743건(17.4%), '가려움증' 21,197건(9.3%), '어지러움' 18,406건(8.0%), '구토' 17,302건(7.6%), '두드러기' 15,932(7.0%) 등의 순으로 많았으며, 2015년과 비교해 상위 5개 증상은 동일하고 일부 순서만 변동됐다.
보고 주체별로 살펴 보면, 지역의약품안전센터가 163,676건(71.5%)으로 가장 많았고, 그 뒤로 제조・수입업체 59,600건(26.0%), 병·의원 3,077건(1.3%), 소비자 2,445건(1.1%) 등의 순이었다.
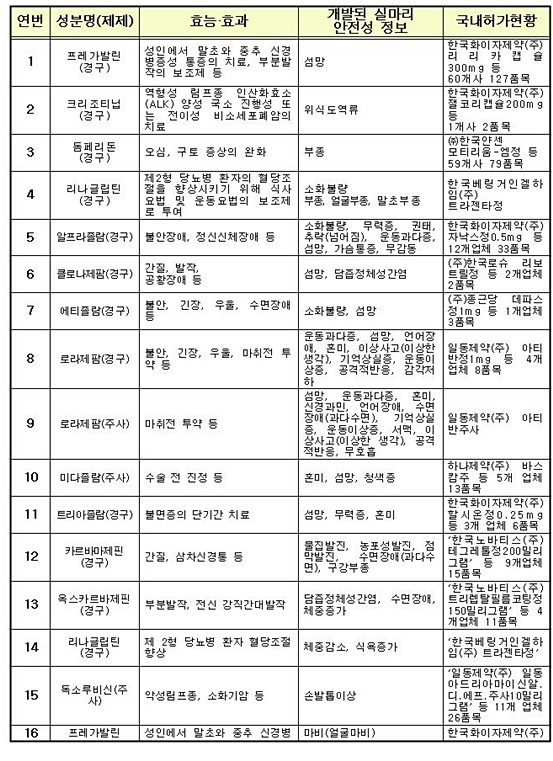
식약처는 2012년 이후 보고된 안전성 정보를 토대로 통계학적 분석과 의약전문가로 구성된 중앙약사심의위원회 자문 등을 거쳐 지난해 부분발작 보조제로 사용되는 '프레가발린' 등 16개 성분 제제(503개 제품)의 허가사항(사용상 주의사항)에 이상반응을 추가하는 안전조치를 취한 바 있다.
또한, 보고된 안전성 정보와 해당 약물의 인과관계를 보다 정확히 확인하기 위해 해당 약물을 사용한 국민의 진료정보, 검사‧처치 등이 포함된 의료 정보와 부작용 보고 자료 연계‧분석을 통해 인과관계 규명의 정확도를 높여나갈 계획이다.
식약처의 '보고자료 분석평가를 통한 허가사항 반영 현황'<下 표 참조>(503개 제품)에 따르면, ▲프레가발린(경구)의 경우, 한국화이자제약 '리리카캡슐 300mg' 등 60개사 127품목, ▲돔페리돈(경구)의 경우, 한국얀센 '모티리움-엠정' 등 59개사 79품목, ▲에티졸람(경구)의 경우, 종근당 '데파스정1mg' 등 1개업체 3품목, ▲로라제팜(주사)의 경우, 일동제약 아티반주사, ▲카르바마제핀(경구)의 경우, 한국노바티스 '테그레톨정200mg' 등 9개 업체 15품목 등이 포함됐다.
| |||||||